 Vaasa, laboratorio-ohjekirja
Vaasa, laboratorio-ohjekirja Vaasa, laboratorio-ohjekirja
Vaasa, laboratorio-ohjekirjaSe även / Ks. myös: Ohjekirjan etusivu | Aakkosellinen luettelo | Aiheenmukainen lista | Päivitykset |Tiedotteet
10.10.2023
HUSLAB, Virologian ja immunologian laboratorio, Neurovirologia ja Elisa -työpiste, puh. 050 427 2126.
HUSLAB, kliininen mikrobiologia, immunologiset tutkimukset.
Tämä on erikoistutkimus josta annetaan lausunto. Tämän johdosta hoitavan lääkärin tulee kirjoittaa edellä mainittuun lähetteeseen diagnoosin kannalta oleelliset seikat.
Mycobacterium tuberculosis (Mtb) aiheuttamat kliiniset ja subkliiniset infektiot, erityisesti vaikeasti diagnosoitavat ekstrapulmonaaliset muodot (luustopesäkkeet, lymfadeniitti, sekä latentin tuberkuloosi (TB) -infektion diagnostiikka), ja varotoimena ennen infektioriskiä lisäävän hoidon aloitusta. Menetelmä soveltuu hyvin lapsipotilaille jo imeväisikäisistä lähtien. Menetelmää voidaan käyttää epäselvissä differentiaalidiagnostiikkaa vaativissa tilanteissa, kuten esim. vaskuliiteissa ja hematologisisen maligniteetin epäilyssä. Negatiivinen tulos ei poissulje TB-infektiota.
Menetelmä on siihen tarvittavan pienen näytetilavuuden vuoksi erityisen sovelias lapsipotilaiden diagnostiikkaan sekä toisaalta tilanteissa, joissa ei voida käyttää B -LyTbIFN, jossa näyte tulee toimittaa tutkivaan laboratorioon 4 tunnin kuluessa.
HUOM! Haponkestävän sauvan värjäys ja viljely ovat edelleen ensisijaisia menetelmiä kliinisissä TB infektioissa. INDIKAATIOT:Testiä käytetään ensisijaisesti M. tuberculosis-tartunnan eli latentin tuberkuloosi-infektion tutkimiseen. Testi voi olla hyödyllinen lisätutkimus aktiivin tuberkuloosin ja etenkin extrapulmonaarisen tuberkuloosin tutkimuksissa. Negatiivinen tulos ei kuitenkaan poissulje aktiivia eikä latenttia TB-infektiota.
HUOM! Haponkestävän sauvan värjäys, nukleiinihaponosoitus ja viljely ovat edelleen ensisijaisia menetelmiä kliinisissä TB-infektioissa.
Putkia voi hakea tai tilata mikrobiologian laboratoriosta p.2842
Näyte esikäsitellään Vaasan keskussairaalan mikrobiologian laboratoriossa.
NÄYTTEENOTTOPÄIVÄT: Ma-to. Arkipyhiä edeltävänä päivänä ei voi ottaa näytettä.
Kevään 2022 poikkeukset:
Juhannuksen 2022 poikkeusaikataulu. Kiireellisissä tapauksissa soittakaa mikrobiologian laboratorioon p. 06 213 2842.
Gammainterferoni, eritys. Entsyymi-immunomenetelmä (EIA). Akkreditoitu menetelmä. B-TbIFNg on immunologinen tutkimusmenetelmä, jolla osoitetaan potilaan verestä M. tuberculosis antigeeneille herkistyneitä T-lymfosyttejä, kuitenkaan niitä erikseen puhdistamatta. Testin erityisnäyteputkessa on M. tuberculosis -bakteerille ominaisia valkuaisaineiden peptidejä, joita ei ole rokotteena käytetyssä BCG-bakteerissa. Peptidit stimuloivat elävän bakteerin aktivoimia "efektori"-T-lymfosyyttejä tuottamaan interferoni gammaa (IFNg). Veren plasmafraktioon tuotettu IFN-gammapitoisuus mitataan EIA-menetelmällä. Tuotettu IFNgamma-määrä on verrannollinen herkistyneiden lymfosyyttien määrään. Verinäytteen lymfosyyttien kelpoisuuden osoituksena käytetään potilaan PHA-stimuloituja soluja (positiivisen kontrollin putki) ja negatiivisena kontrollina toimivat potilaan stimuloimattomat solut.
3-4 kertaa viikossa.
Kvantitatiivinen tulos on valmiina 4 työpäivän kuluessa. Kiireellisistä näytteistä voidaan sopia erikseen.
Erikoisnäytteenottoputkia (4 kpl) voi hakea tai tilata mikrobiologian laboratoriosta p.2842
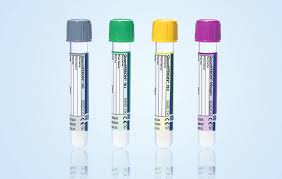
Tarkista aina putken kelpoisuusaika!
Näytteenottojärjestys: Nil (harmaa), TB1 (vihreä), TB2 (keltainen), Mitogen (violetti).
TARROITUS: Liimaa kaikki tulostuneet osatutkimustarrat tarroja vastaaviin putkiin ennen näytteenottoa seuraavasti: B -NIL -tarra harmaaseen putkeen (Nil), B- TB1 vihreään (Tb1), B-TB2 keltaiseen (Tb2) ja B-MITO violettiin (Mitogen). Lopuksi laita päätutkimustarra (B-TbIFNg-tarra) pystyyn/pitkittäin violettiin Mitogen-putkeen osittain B-MITO -tarran päälle niin ettei B-MITO-tarran viivakoodi kuitenkaan peity.
HUOM! Ota näytettä mustaan merkkiviivaan asti (validoitu näytetilavuus 0,8 - 1,2ml). Huomioi tämä avo-/ siipineulalla otettaessa. Käännä putkia 8-10 kertaa ylösalaisin niin että koko sisäpinta kastuu verellä, koska antigeenit ovat kuivattuina putkien sisäpinnoille. Perhosneulalla otettaessa tulee ottaa ns. hukkaputki ennen varsinaisia näytteitä.
4 x 1.0 ml (0,8-1,2 ml)
Veriputket pidetään huoneenlämmössä, niitä ei saa laittaa jääkaapiin eikä pakastaa. !Säilyy sentrifugoituna viikonlopun yli, ei oteta rutiinisti perjantaisin.
Ma-pe huoneenlämmössä, oltava perillä 3 vrk:n kuluessa. Lähetys primääriputkessa; plasmaa ei tarvitse erottaa. Hemolyysi putkessa ei haittaa. Juhannusviikolla (vko 25) näytteiden lähetys vain ma 15.6.-ke 17.6.
Aluelaboratoriot: lähettäessänne putket VKS:ään, laittakaa ne muovipussiin ja mukaan lappu, jossa lukee onko inkubaatio jo tehty vai ei!
alle 0.35 IU/ml
Viitealue:
| Reaktiivinen | 0.50 IU/ml |
| Raja-arvoinen | 0.35-0.50 IU/ml |
| Non-reaktiivinen | alle 0.35 IU/ml |
Positiivisen tuloksen katsotaan merkitsevän joko aktiivia tai latenttia TB-infektiota.
Reaktiivisiin tuloksiin liittyy lausunto. M. tuberculosis-infektion lisäksi harvinaiset M. marinum, M. kansasii ja M. szulgai - infektiot voivat myös antaa positiivisen tuloksen. Yleisesti ottaen reaktion peptideille voidaan katsoa olevan spesifi eikä BCG-rokotus aiheuta positiivista tulosta.
HUOM! Negatiivinen tulos (non-reaktiivinen) ei sulje pois aktiivin tuberkuloosin mahdollisuutta. Erittäin vaikeassa TB- infektiossa ja vahvasti immunosuppressoiduilla potilailla negatiivinen tulos on mahdollinen mutta harvinainen.
Lymfopenian yhteydessä tulosten tulkinta on epävarmaa. B - TbIFNg -tutkimusta suunniteltaessa on suositeltavaa mitata lymfosyyttien taso puutteelle altistavissa kliinisissä tilanteissa. Lymfopeniapotilailla B -LyTbIFN (6174) on suositeltavampi testi herkistymisen osoittamiseksi.
Kun esiintyy voimakkaampaa spontaania IFN-gammaeritystä (nollaputki=Nil >1 IU/ml), laboratorio toistaa tuloksen harkinnan perusteella, ja ottaa huomioon sen tuloksessa ja lausunnossa. Taustastimulaatio voi johtua potilaan muusta samanaikaisesta infektiosta tai näytteen ottamiseen/ käsittelyyn liittyvästä teknisestä ongelmasta.
Jos kontrollimitogeeniputki ei anna YLI 0.50 IU/ml- ylittävää tulosta, jää potilaan lymfosyyttien toimintakyky epäselväksi eikä reaktiotulosta M. tuberculosis-antigeeneille voi antaa.
Ammattilaisneuvonta Pohjanmaa 041 7314 786
*25.8.2016 Näyteastiamuutos.
*16.12.2016 Korjattu näytteenotto- ja lähetyspäivät
*23.9.2019 Lisätty tarroitusohje
*7.10.2019 Poistettu laboratorion ohjeesta sentrifugointi.